 醫學研究部(Department
of Medical Research)
醫學研究部(Department
of Medical Research)共 同 研 究 室 電 子 報
第133期 Jan.10.2025
本期目錄
下期主題
快速連結
本期電子報介紹如何利用器官芯片技術,提供精確模擬人體生理特徵的解決方案,並助力藥物評估和疾病研究。目前,相關廠商提供多種經過驗證的器官芯片系統,可供同仁開發使用。下一期電子報主題為[單細胞蛋白質體技術],敬請期待,並竭誠歡迎您訂閱共同研究室電子報以收取儀器介紹、研究新知、與每月訓練課程資訊,更歡迎您與我們聯絡,給予我們建議與鼓勵。
TOP
進階生物科技公司 楊介文經理
器官芯片的開創性工作是由哈佛大學WYSS 研究所的系主任Donald E.Ingber院士團隊完成的,其在Science發表了器官芯片領域具有里程碑意義的第一個成功的模型:肺芯片。之後Emulate公司成立,將器官芯片技術商業化運行,與更廣泛的生命科學界同仁分享這一精妙的器官芯片技術。自成立以來致力於開發高度模擬人體生理特徵的器官芯片技術和不同類型的創新應用,以全面了解疾病發生規律和幫助評估藥物的真實反應,改善人類健康。目前,Emulate提供經過驗證的肝、腎、十二指腸、結腸、肺、腦等器官芯片解決方案的同時支持客戶定制化的研究需求,是全球市場佔有率領先的器官芯片品牌。全球系統裝機量超過400台,已經被全球排名前20的藥廠全部合作引入,採用Emulate人體仿真係統發表的文章數已超過100篇,在同類產品中大幅領先。Emulate相信,人類生物學和器官芯片技術的結合能夠點燃人類健康的新時代。
動物模型局限性
受限於藥物代謝酶和細胞轉運體的物種差異,以及調節轉錄啟動的機制不同,動物模型的資料難以推導到臨床。例如,在小鼠中,參與藥物代謝的主要基因家族中有 34 個細胞色素 P450(CYP),即 CYP1A、CYP2C、CYP2D 和 CYP3A 基因簇,而在人類中只有 8 個。有趣的是,三種人類酶,CYP2C9、CYP2D6 和 CYP3A4,占所有反應的 75%,其中 CYP3A4 是唯一最重要的人類 CYP450,占人類第一階段藥物代謝的 45%。此外,許多主要的人類 CYP450 酶和藥物轉運體(決定藥物暴露的水準和變化)的表達水準受多種轉錄因數的控制,這些重要的因素均表現出明顯的物種差異。加上腸道和肝臟中藥物代謝酶和藥物轉運體之間複雜的相互作用,以及底物和抑制劑特異性的重疊,使得在藥物開發的臨床前階段很難預測人類藥代動力學。
2D 細胞局限性
目前已有一些臨床前體外非動物模型被應用於潛在候選藥物在人體中的吸收、分佈、代謝和排泄(ADME)的描述和預測。其中,Caco-2單層培養在transwell嵌件上,作為人類小腸的體外代表,它是整個製藥業使用最多的模型之一。然而,缺乏體內相關的三維(3D)細胞結構,缺乏適當的細胞群比例,藥物轉運體和藥物代謝酶的表達譜改變(尤其是CYP450 酶家族),以及異常的 CYP450 誘導反應,對使用這些傳統模型來預測人類在臨床上的反應提出了挑戰。
3D類器官球局限性
隨著3D類器官的技術的發展,替代傳統單層細胞培養的方法已逐漸顯現。使用3D類器官,可應用多種不同的研究方向,包括器官發育、疾病建模和再生醫學。然而,3D類器官在藥代動力學研究仍然非常有限。主要局限性為類器官的3D球體緻密導致其球體內部細胞的滲透性降低,甚至很多內部細胞已經缺氧而死亡,導致評估整個球體的滲透性或藥物吸收性能大打折扣。此外,傳統培養3 D類器官球是非常耗時耗力的過程,並且球的外表面細胞通常被非常厚的基質膠(如Matrigel)所包埋,可能會進一步限制藥物的滲透。同時,體外無序培養而成的器官結構,其大小、形狀和活力方面的異質性,造成難以統一和標準化,也會阻礙藥代動力學的研究。
傳統動物實驗與器官晶片的差異
-
受限於藥物代謝酶和細胞轉運體的物種差異,以及調節轉錄啟動的機制不同,動物模型的藥代動力學資料難以推導到臨床。
-
傳統3D腸道類器官球體內部緻密,並且周身包圍於基質膠,藥物難以滲透。加上靜態體系中的無序培養,不同球體在大小、形狀、結構上差異巨大,難以標準和統一化,導致研究藥代動力學和藥物相互作用困難巨大。
-
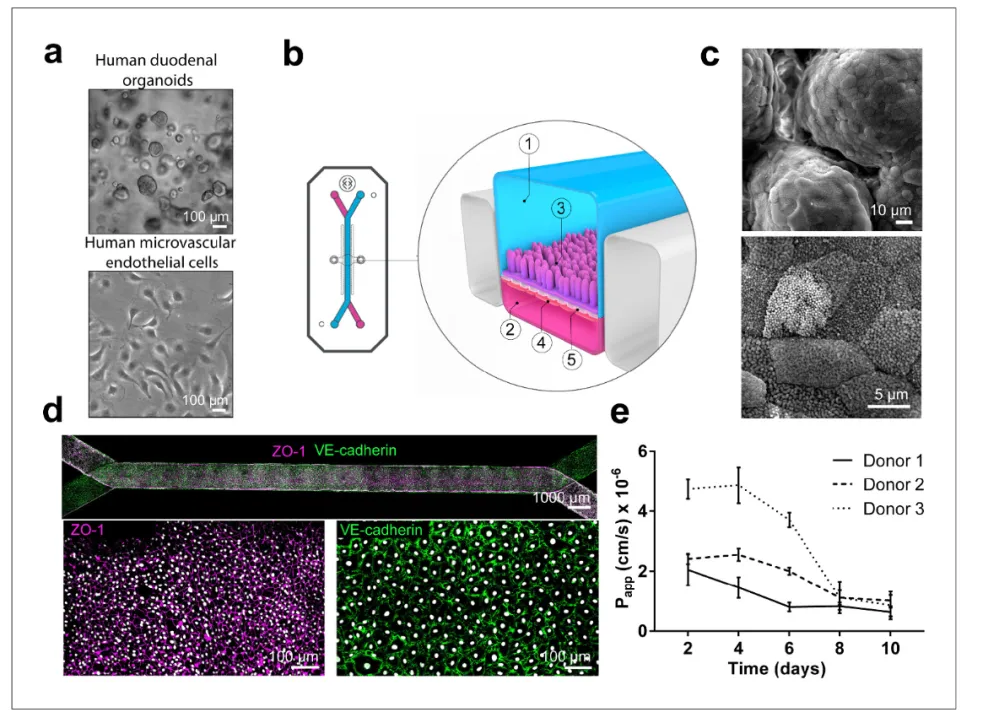
Emulate的研究人員開發了原代十二指腸器官晶片模型,類比腸道組織結構和功能,用於研究藥代動力學和藥物相互作用。並且作為標準化的商品,可供用戶迅速在自己實驗室建立模型。
Emulate器官晶片優勢
本研究中,Emulate 的研究人員開發了原代十二指腸器官晶片模型,類比腸道組織結構和功能,用於研究藥代動力學和藥物相互作用。十二指腸腸道晶片顯示了高度成熟,且與生理相關度更高的極化上皮細胞結構,並呈現出與體內類似的屏障功能。轉錄組學分析表明,相比于單層細胞和3 D 類器官體系,器官晶片的基因表達譜與體內更為接近,尤其是針對於藥物轉運和代謝相關的分子。與單層細胞的器官晶片培養體系相比,Emulate十二指腸器官晶片模型顯示出更好的CYP3A4表達和誘導能力。重要的是,將 Emulate十二指腸腸道晶片暴露於CYP450誘導劑,如利福平和骨化三醇,導致 CYP3A4 mRNA、蛋白質水準和藥物代謝活性明顯增加。我們的結果表明,3D 類器官衍生的十二指腸細胞可以與Emulate器官晶片技術相結合,為CYP450介導的代謝、藥物轉運體的活性和藥物相互作用風險的臨床前評估提供一個強大平臺。Emulat e 標準化的十二指腸器官晶片模型的建立可以更好地預測人類藥代動力學和藥物相互作用風險。
肺器官晶片的特點
呼吸道粘膜表面通過粘液纖毛清除不斷清除吸入空氣中的污染物,這是防止肺部感染和損傷的重要防禦機制。這一功能依賴於特化上皮細胞的組合,這些細胞利用運動的纖毛將分泌的粘液和滯留在空氣中的物質運出氣道。靜態培養條件無法通過實驗控制上皮向不同氣道分支特有的細胞組成分化。這限制了人氣道上皮細胞模型的研究轉化價值,尤其是在研究感染性病原體如何破壞成熟的黏膜纖毛清除,以及為什麼某些疾病會主要影響大氣道或小氣道的機制探索。
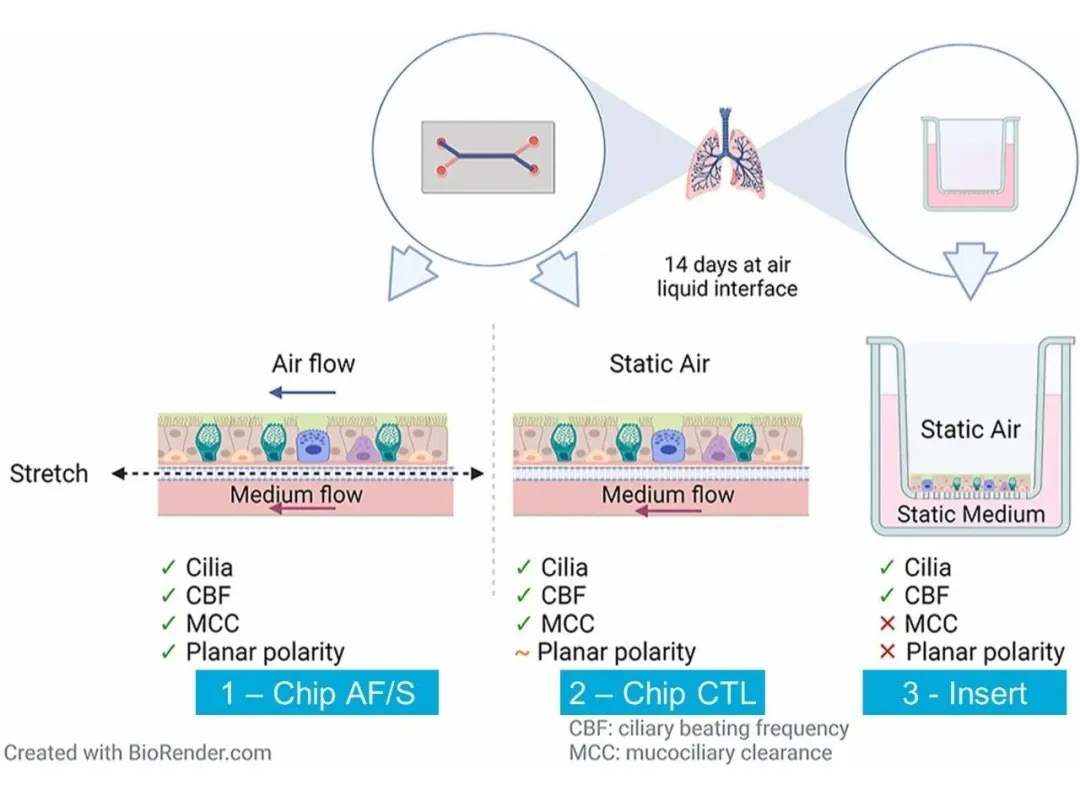
與呼吸有關的機械應力,包括拉伸應力和剪切應力,在體內肺上皮組織的整個發育過程中都會產生重要作用,在大氣道和小氣道中的作用程度不同,並能在體外改善氣道上皮屏障功能。為了探索正常呼吸相關氣流剪切力和應變可調節人原發性支氣管上皮細胞(hPBEC)的粘膜功能和發育機制,本文採用了三種不同的實驗模型:利用Emulate氣道器官晶片構建含有可拉伸多孔膜和氣液介面(ALI)的分化hPBEC的方案,可以模擬拉伸作用力和氣流剪切力 (1-Chip AF/S);缺乏拉伸和氣流剪切力,但納入培養基液流的初代氣道模型 (2-Chip CTL);傳統的插入式細胞培養模型則是完全靜態的(3- Inser t)。利用不同模型,本文評估了粘液纖毛清除功能和氣道上皮在動態微流控環境下的分化情況。
機械應力促使細胞分化
利用Emulate Chip-S1器官晶片,活化後的中間膜層包被IV型膠原ECM蛋白然後接種hPBEC後,可在頂部通道形成細胞粘附和匯合單層。初期培養基浸沒培養階段,頂部和底部通道對hPBEC進行動態培養基灌注;然後在頂部通道切換到氣液介面(ALI)以啟動分化,同時在底部通道繼續進行培養基灌注(圖 1A 部)。成熟氣道上皮的一個核心功能標記:是粘液纖毛清除(MCC)。文章通過跟蹤螢光微珠在纖毛上皮細胞中的位移來直接評估MCC的功能。儘管跳動頻率相似,但器官晶片中的MCC明顯優於靜態插入式培養。器官晶片中,MCC的總表面積比例明顯更高,從而使組織平均MCC速度提高了一倍(圖2C-E)。這些表明,在器官晶片上培養hPBEC並結合氣流和拉伸可提供關鍵的環境線索,促進體外多纖毛氣道上皮細胞的功能成熟。


| 01月15日 |
螢冷光膠體影像分析儀(ThermoFisher iBright)實機示範操作課程 |
| 01月21日 | Single Cell Analysis Technologies and High Efficient Solutions--單細胞分析技術及其高效解決方案 |
歡迎您訂閱共同研究室電子報以收取儀器訓練與研究新知課程講習相關資訊 。
為持續提供優質之研究服務,便於日後聘用專職技術人員、購置新儀器、現有儀器汰舊換新與維護保養等等,敬請於使用共同研究室資源並發表論文時,於論文致謝(Acknowledgement)處加入致謝共同研究室之文句,並於論文發表時通知共同研究室管理人員。致謝文句請依實際使用情形書寫,或請參考以下範例:We
thank the staff of the Core Labs, Department of
Medical Research, National
Taiwan University Hospital for
technical support.