 醫學研究部(Department
of Medical Research)
醫學研究部(Department
of Medical Research)共 同 研 究 室 電 子 報
第115期 JUL.10.2023
本期目錄
下期主題
快速連結
為推動再生醫療發展讓更多病人受惠,衛福部推動「再生醫療雙法」修法,在推動法案前提需有強大再生醫療技術與製劑技術管理,並確保再生醫療品質跟安全有效性,以及維護病人權益,本期邀請樂迦再生科技醫療長介紹如何建構醫療技術團隊,讓讀者了解細胞治療技術培育歷程與挑戰。下一期電子報主題為「海馬生物能量分析儀低氧下的生物能量代謝檢測」,敬請期待,並竭誠歡迎您訂閱共同研究室電子報以收取儀器介紹、研究新知、與每月訓練課程資訊,更歡迎您與我們聯絡,給予我們建議與鼓勵。
TOP
樂迦再生科技醫療長 張裕享醫師
如何跨越死亡之谷?
不知道各位科學家讀者有沒有這種感嘆? 空有滿腹的科學創新,做了老鼠實驗發表在很棒的國際期刊,但卻無法治療病人?
2008年Nature雜誌就發表一篇文章,標題是Crossing the Valley of Death,提到科學家們有很好的研究創新,病人也有許多急需解決的醫療需求,但在科學家和病人之間卻存在著死亡之谷讓人望之卻步! (圖一) 時至今日,問題解決了沒? 答案是沒有,Attila這位美國布朗大學的學者在2019年在國際期刊仍指出,現在學界走向企業商品化之路,死亡之谷仍然擋在兩者中間,包括經費、智財權、臨床試驗、法規、製程等等都可能發生問題。而這些複雜的問題,往往不是長年在學術界的科學家能夠解決的。

圖一.
跨越死亡之谷
第一個CAR-T細胞從實驗室到細胞產品走了多久?
答案是14年,這個答案可能嚇到您了,真的需要這麼久的時間?
時間回到2003年,我的恩師Dario Campana和他實驗室裡日本小兒血液科醫師Dr. Imai,一位每天工作17小時的傳奇人物,在美國St Jude兒童研究醫院的實驗室發明了第一個CD19BBz CAR序列, Dr. Campana回憶那時候在美國血液病大會(ASH meeting)口頭報告這個驚天動地的發現時,諾大的場地裡只有13個聽眾。對比今日,動不動就是數千人的CAR-T研討會,真是不可同日而語。這個發明於2004年發表在Leukemia這個期刊。後來賓州大學的Carl H. June跟Dr. Campana簽訂Material Transfer Agreement,將此CAR DNA序列拿去研究,後來在2011年新英格蘭醫學雜誌發表一位CAR-T成功治療的慢性淋巴性白血病病人Bill Ludwig,從此Carl H. June聲名大噪,後來將此CAR-T細胞治療授權給諾華大藥廠,於2017年美國FDA通過了人類歷史上第一個CAR-T細胞治療Kymriah,一袋細胞要價47.5萬美元。在美國一流的醫院和大藥廠仍需要14年才能將實驗室的發明推到細胞產品,您覺得這種情況如果是科學家的您需要花幾年的功夫呢?
專業細胞製造團隊可縮短CAR-T新藥開發時程:
上述的實例說明CAR-T新藥開發不只是時間漫長,也因為製程的困難造成發展的過程像是接力賽—一棒接一棒。細胞製程有三個困難之處。首先是製造過程有多種儀器需要選擇;再者有多種基因改造的方式,例如病毒載體轉染、跳躍基因及基因編輯的方式;最後是每個步驟都有多種試劑須選擇決定,上述不同的製造選項加起來有很多的排列組合,製造的過程也因為細胞量大、等級高,所以所費不貲。因此如何在短時間內製造出最佳特性的CAR-T細胞,就非常依賴專業的CDMO團隊協助CAR-T細胞製造。也因為如此,歐美的統計資料顯示,研發型CAR-T細胞公司正與CDMO公司合作,僅23%完全自行生產。這種高度專業的細胞代工製造就如同台積電之晶圓代工,上下游垂直分工應在未來該是擋不住的趨勢。
CAR-T製程代工的三大挑戰
CAR-T製程與細胞代工未來面臨許多挑戰,首先是異體CAR-T細胞,異體CAR-T細胞的好處之一,是藉由事先生產提供者的CAR-T細胞,現成的細胞產品可即時治療許多病況緊急的病人。此外,藉由大量生產也能使藥價降至合理的範圍。但異體CAR-T最大的困難是排斥問題,即使做了極複雜的基因改造,異體CAR-T細胞治療也普遍存在持續性不佳的問題;挑戰之二是縮短製程時間,透過縮短製程可以減少病人在等待過程中病情惡化的可能,另外還有因為縮短製程使T細胞更年輕,療效更好,然而在縮短製程的同時,產品相關參數變化的挑戰就產生了;最後是國際化的問題,這個是所有在台灣生技公司普遍存在的挑戰。樂迦再生積極網羅專家學者打造國際化的團隊,如古石和親他是CDMO公司Minaris的前執行長,擁有建廠和執行業務相關的能力;另外還聘請CD19 CAR序列發明人Dario Campana擔任科學顧問Dario Campana (圖二)曾在美國小兒血液科排名第一的醫院St Jude兒童研究醫院服務長達20年,2000年之前,他首創MRD (Minimal Residual Disease)技術,利用流式細胞儀精準檢測血癌病人骨髓裡微量殘存的血癌細胞,除了可以預測病人預後之外,重要的是能夠根據檢驗結果調整後續的治療,例如加強化療,或增加標靶治療,甚至做異體血液幹細胞移植。國內數家醫學中心的醫師都曾經到Dr. Campana實驗室學習MRD技術,應用到血癌病人常規檢驗之中。Dr. Campana擁有多個細胞治療專利,有專利不稀奇,能夠應用到病人並且有效才厲害。2003年之後Dr. Campana開始投入細胞治療,第一個發明就是上述的世界第一個CD19BBz CAR序列,這個專利分別授權給Novartis的CAR-T細胞產品Kymriah,還有BMS的Breyanzi,廣泛應用於全世界的血癌淋巴瘤病人。後續他還有數個細胞治療專利,目前在新加坡大學執行臨床試驗,三顧集團將這些CAR-T技術引進台灣,造福台灣的病人。

圖二. 在新加坡大學與Dr. Campana合影(2023.5.16)
打造再生醫療生態系
國內半導體產業的成功模式是「垂直分工」,分工合作造就生氣蓬勃的半導體產業鏈生態系。反觀國內生技產業,少有生技公司有分工合作爭取國際訂單的情事,這是非常可惜的事情。尤其是我國醫療技術世界第三,擁有優秀的臨床醫師及豐沛的醫療資源,是再生醫療發展的最佳環境,應上下游分工,打造優質CDMO團隊。好的CDMO團隊除了具備成功製造CAR-T細胞的經驗,提供客戶選擇不同的製程平台之外,並應建立法規單位通過三期臨床試驗之前導工廠,有專業品保、品管、製程開發人才,可協助國內外研發團隊,量身訂做最好的CAR-T細胞製程,CDMO團隊專注於開發新製程平台,不和客戶競爭做新藥開發,客戶可放心地把研發多年的CAR-T專利交給該團隊生產,分工合作,透過創新、合併、協同進化,共享資源創造台灣再生醫療生態系,加速台灣再生醫療研發從實驗室進入臨床應用,步上國際舞台(圖三)。
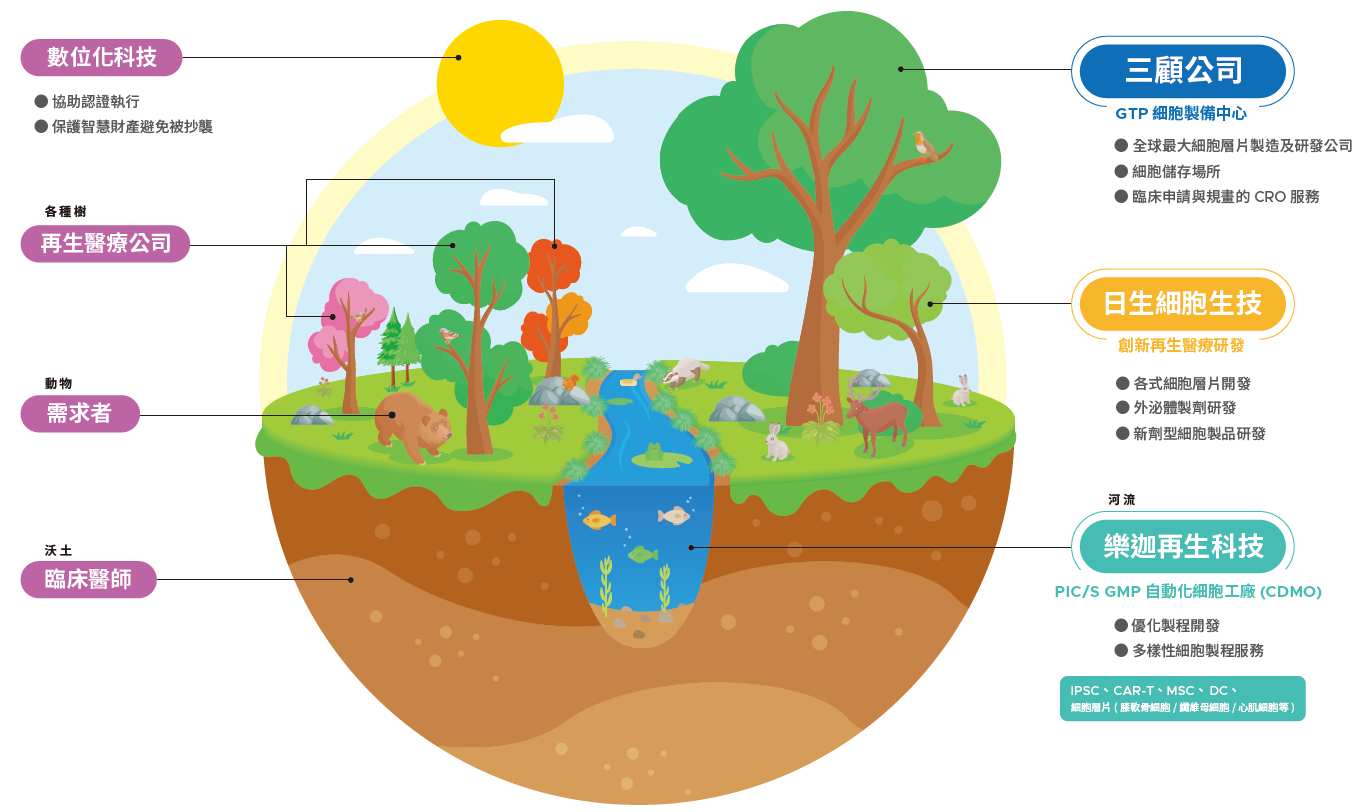
圖三.
打造台灣再生醫療生態系
貴重儀器訓練課程:課程網路報名
| 07月21日 | BD Verse流式細胞儀實機教學/認證課程 |
研究新知課程:課程網路報名
| 07月11日 | 自動化western平台-Simple Western系統原理與介紹 |
歡迎您訂閱共同研究室電子報以收取儀器訓練與研究新知課程講習相關資訊 。
為持續提供優質之研究服務,便於日後聘用專職技術人員、購置新儀器、現有儀器汰舊換新與維護保養等等,敬請於使用共同研究室資源並發表論文時,於論文致謝(Acknowledgement)處加入致謝共同研究室之文句,並於論文發表時通知共同研究室管理人員。致謝文句請依實際使用情形書寫,或請參考以下範例:We
thank the staff of the Core Labs, Department of
Medical Research, National
Taiwan University Hospital for
technical support.